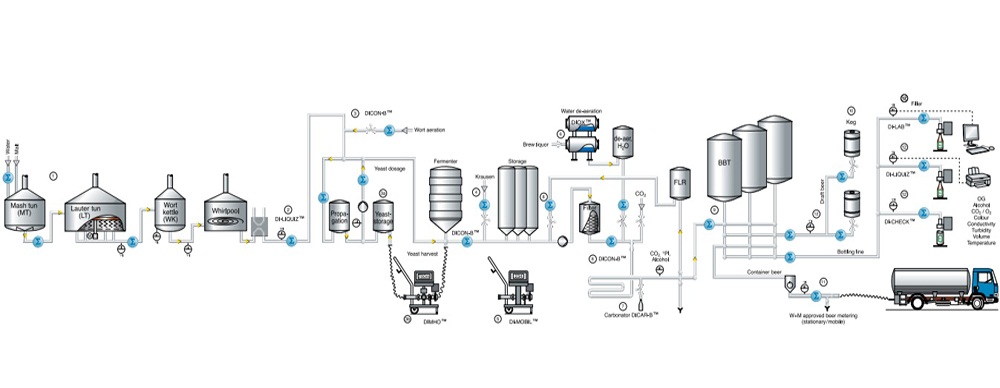
Validación y verificación Servicios (V & V)
BIOFLUID ofrece servicios de BPM como parte de la calificación y validación de plantas, sistemas de informática y procesos en la industria farmacéutica, consultoría para la implantación de procesos que cumplen con GMP en ingeniería y producción, Calificación y Validación
- La realización de la evaluación básica y detallada de Riesgos
- Vendor Qualification & Procurement asistencia
- Preparación del plan maestro de validación
- Preparación de Informes DQ, IQ y OQ protocolos e informes
- Cualificación de la ejecución
- La validación del proceso
- Validación de la limpieza
- La planificación, coordinación y ejecución de todas las actividades de calificación / validación
- La validación de los sistemas informáticos
La validación del proceso:
Con el fin de hacer un uso óptimo de personal y recursos técnicos, es aconsejable planificar temprano para proyectos de validación. Es necesario coordinar de manera óptima el desarrollo, los procesos, la caracterización de productos, producción y aseguramiento de la calidad con el fin de lograr el mejor rendimiento general del proyecto es posible que no deja huecos y evitar redundancias.
Le apoyamos en la implementación de la calidad por diseño (QbD) con las herramientas más importantes que son necesarios para este: Diseño de Experimentos (DOE) y los análisis de riesgo de conducción. Definición adecuada y la clasificación de su funcionamiento y aceptación rangos, así como los límites de alerta y de acción asociado garantizan un control óptimo del proceso.
- Proporcionamos apoyo para el diseño y la coordinación de su proyecto de validación
- Ofrecemos servicios de consultoría y coordinación, así como la creación de análisis de riesgo / evaluaciones, así como documentación de validación (documentos originales) para los estudios de consistencia.
- Ofrecemos estudios de estabilidad de los medios de comunicación, tampones de procesos y productos intermedios del proceso
Ofrecemos estudios de estabilidad de los medios de comunicación, tampones de procesos y productos intermedios del proceso :
- la planificación de las plantas de fabricación compatibles con GMP
- cualificación planta y validación informática
- cualificación planta y validación informática
- validación de métodos analíticos
- elaboración de procedimientos normalizados de trabajo
- la formación de sus empleados
Computer Validación:
Coordinamos la validación de los sistemas a lo largo de todo el ciclo de vida.
Los sistemas automatizados que afectan a la calidad del producto y el producto de seguridad de los productos farmacéuticos deben cumplir con los requisitos de las normas GMP y deben ser validados.
Planes BIOFLUID y coordina la validación de los sistemas automatizados de acuerdo con normas de la UE y de los Estados Unidos y / o de acuerdo con los requisitos de las autoridades nacionales.
Definimos medidas de validación adecuados para su sistema que se personaliza para el riesgo para la calidad y seguridad de sus productos, y coordinamos la validación de los sistemas a lo largo de todo el ciclo de vida.
Le apoyamos en el:
- definición de la criticidad GMP de sus sistemas (ejecución de riesgo del sistema analiza)
- preparación de planes maestros de validación según GAMP5
- desarrollo de planes de calidad y de proyectos
- ejecución de riesgo funcional analiza según FMEA definición del ámbito de aplicación de la prueba, basado en el riesgo
- ejecución de 21 CFR Parte 11 evaluaciones
- coordinación de la fase de prueba en el proyecto
- coordinación de la gestión del cambio en el proyecto
- evaluación y revalidación de los sistemas ya existentes
- preparación de los procedimientos normalizados de trabajo necesarios
- la formación de sus empleados
- Hacer uso de la consultoría para mantener el estado validado de sus sistemas automatizados durante las operaciones (gestión de cambios, gestión de la configuración)